一場世界一場戰鬥
─建立一個全球共同命運社區的國際合作,以應對COVID-19的大流行挑戰
全世界席捲全球的新穎冠狀病毒導致了一場持續的全球互聯19日大流行危機。這部小說的冠狀病毒沒有邊界,沒有任何國家能夠擺脫與Covid-19的這場戰鬥。為了回應這一世界範圍的Covid-19大流行,Liming Bio-Products Corp正在為支持我們全球社區的福祉做出貢獻。
目前,我們的世界面臨著新型冠狀病毒疾病2019(COVID-19)大流行的前所未有的影響。迄今為止,尚無有效的藥物來治療該疾病。但是,已經開發了許多診斷測試以檢測COVID-19。這些測試基於分子或血清學方法,用於檢測新型冠狀病毒特異性核酸或抗體生物標誌物。由於Covid-19達到了大流行狀況,因此對新型冠狀病毒感染的早期診斷對於評估病毒的傳播並包含該病毒至關重要,但是對於普遍使用的完美測試尚不存在。我們必須知道哪些測試有可能用於篩查,診斷和監測Covid-19感染,以及它們的局限性是什麼。如何更好地利用這些科學工具並幫助識別和控制這種迅速傳播和嚴重疾病的出現非常重要。
檢測新型冠狀病毒的目的是確定患有COVID-19感染的人還是可能默默傳播病毒的漸近載體,以提供基本信息來指導臨床治療的決策。先前的研究表明,70%的臨床決策取決於測試結果。當使用不同的檢測方法時,檢測試劑試劑盒的要求也不同。
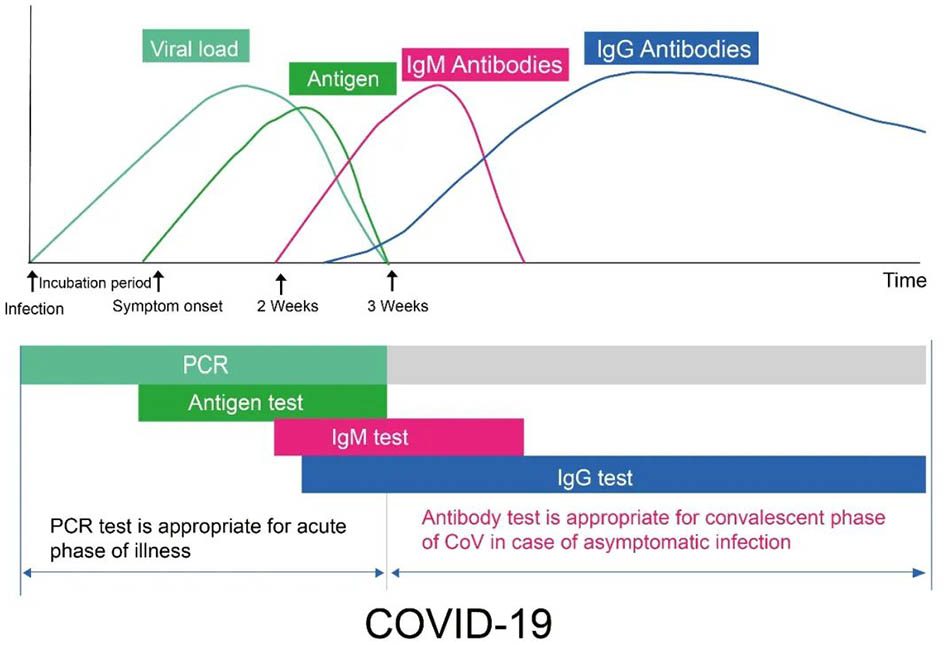
圖1
圖1:圖顯示了在Covid-19感染的典型時間過程中一般生物標誌物水平的關鍵階段。 X軸表示感染天數,Y軸表示不同時期內的病毒載量,抗原濃度和抗體濃度。抗體是指IgM和IgG抗體。 RT-PCR和抗原檢測都用於檢測新型冠狀病毒的存在或不存在,這是早期患者檢測的直接證據。在病毒感染的一周內,首選PCR檢測或抗原檢測。在新型冠狀病毒感染約7天后,針對新型冠狀病毒的IgM抗體在患者的血液中逐漸增加,但存在的持續時間很短,其濃度迅速降低。相反,通常在病毒感染後大約14天后,針對病毒的IgG抗體出現。 IgG濃度逐漸增加,並且在血液中持續很長時間。因此,如果在患者的血液中檢測到IgM,則意味著該病毒最近已感染,這是早期的感染標記。當患者的血液中檢測到IgG抗體時,這意味著病毒感染已有一段時間了。它也稱為晚期感染或先前的感染。在恢復階段的患者中通常可以看到它。
新穎冠狀病毒的生物標誌物
新型冠狀病毒是一種RNA病毒,由蛋白質和核酸組成。該病毒侵入宿主(人體),通過結合位點對應受體ACE2進入細胞,並在宿主細胞中復制,導致人免疫系統對外國入侵者反應並產生特定的抗體。因此,從理論上講,小絲核酸和抗原以及針對新型冠狀病毒的特異性抗體可以用作檢測新型冠狀病毒的特定生物標誌物。對於核酸檢測,RT-PCR技術是最常用的,而血清學方法通常用於檢測新型冠狀病毒特異性抗體。當前,我們可以選擇多種測試方法來測試COVID-19感染[1]。
新型冠狀病毒主要測試方法的基本原理
到目前為止,可用於COVID_19的許多診斷測試,每天都在緊急使用授權下獲得更多的測試套件。儘管新的測試開發具有許多不同的名稱和格式,但所有當前的CoVID_19測試基本上都依賴於兩種主要技術:病毒RNA的核酸檢測和血清學免疫測定,可檢測病毒特異性抗體(IgM和IgG )。
01。核酸檢測
逆轉錄聚合酶鏈反應(RT-PCR),環介導的等溫擴增(LAMP)和下一代測序(NGS)是檢測新型冠狀病毒RNA的常見核酸方法。 RT-PCR是世界衛生組織(WHO)和美國疾病控制與預防中心(CDC)推薦的COVID-19的第一類測試。
02.系統抗體檢測
抗體是針對病毒感染而在人體中產生的保護蛋白。 IgM是抗體的早期類型,而IgG是後期類型的抗體。通常檢查血清或血漿樣品是否存在特定的IgM和IgG類型的抗體,以評估COVID-19感染的急性和恢復階段。這些基於抗體的檢測方法包括膠體金免疫色譜法,乳膠或熒光微球免疫色譜法,酶聯免疫吸附測定法(ELISA)和化學發光測定法。
03.病毒抗原檢測
抗原是人體識別的病毒結構,它觸發免疫防禦系統以產生從血液和組織中清除病毒的抗體。可以通過使用免疫測定法靶向和檢測到病毒上的病毒抗原。像病毒RNA一樣,病毒抗原也存在於感染個體的呼吸道中,可用於診斷COVID-19感染的急性期。因此,通常建議收集上呼吸道標本,例如唾液,鼻咽和口咽拭子,深咳嗽痰,支氣管肺泡灌洗液(BALF)進行初始抗原測試。
選擇新型冠狀病毒的測試方法
選擇測試方法涉及許多因素,包括臨床環境,測試質量控制,周轉時間,測試成本,採樣收集方法,實驗室人員技術要求,設施和設備要求。核酸或病毒抗原的檢測是提供病毒存在的直接證據,並確認新型冠狀病毒感染的診斷。儘管有許多用於抗原檢測的方法,但它們對新型冠狀病毒的檢測敏感性在理論上低於RT-PCR擴增的敏感性。抗體測試是在人體中產生的抗病房抗體的檢測,該抗體在時間滯後,通常不能在病毒感染的急性期間用於早期檢測。檢測應用的臨床環境可能會有所不同,樣品收集位點也可能不同。為了檢測病毒核酸和抗原,需要在存在病毒的呼吸道中收集樣本,例如鼻咽拭子,口咽拭子,痰液,痰液或支氣管肺泡灌洗液(BALF)。對於基於抗體的檢測,需要收集並檢查血液樣本,以便存在特定的抗病毒抗體(IgM/IgG)。但是,抗體和核酸測試結果可以相互補充。例如,當測試結果是核酸陰性,IgM陰性但IgG陽性時,這些結果表明患者目前沒有攜帶該病毒,但已從新型的冠狀病毒感染中回收。 [2]
新型冠狀病毒測試的優點和缺點
在新型冠狀病毒肺炎的診斷和治療方案中(試驗版本7)(由國家衛生委員會和國家中醫國家管理於2020年3月3日發布),將核酸測試用作診斷新穎的金標準方法冠狀病毒感染,而抗體測試也被認為是診斷的確認方法之一。

病原和血清學發現
(1)致病結果:使用RT-PCRAND/或NGS方法,可以在鼻咽拭子,痰,下呼吸道分泌,血液,糞便和其他標本中檢測到新型冠狀病毒核酸。如果從下呼吸道(痰液或空氣區提取)獲得標本,則更準確。收集後應盡快提交樣品進行測試。
(2)血清學發現:發作後3-5天左右可檢測到NCP病毒特異性IgM;與急性相比,IgG在康復期間至少增加了4倍的滴定。
但是,測試方法的選擇取決於地理位置,醫療法規和臨床環境。在美國,NIH發布了2019年冠狀病毒疾病(COVID-19)治療指南(現場更新:4月21日21020年4月21日),FDA發布了2019年冠狀病毒疾病診斷測試的政策,2019年在公共衛生緊急情況下(於3月16日發布) ),其中僅選擇作為篩查測試的IgM/IgG抗體的血清學檢測。
核酸檢測法
RT_PCR是一種高度敏感的核酸測試,旨在檢測呼吸道或其他樣本中是否存在新型冠狀病毒RNA。 PCR陽性測試結果是指樣品中存在新型冠狀病毒RNA,以確認COVID-19的感染。負PCR測試結果並不意味著缺乏病毒感染,因為它可能會受到恢復階段的樣本質量或疾病時間點的影響。儘管RT-PCR是一個高度敏感的測試,但它具有幾個缺點。 RT-PCR測試可能是勞動力密集型且耗時的,至關重要的是樣本的高質量。這可能是一個挑戰,因為病毒RNA的量不僅在不同的患者之間差異很大,而且在同一患者中可能會有所不同,具體取決於收集樣品以及感染階段或臨床症狀發作的時間點。檢測新型冠狀病毒需要高質量的標本,其中包含足夠數量的完整病毒RNA。
RT-PCR測試可能會給某些患有COVID-19感染的患者帶來不正確的陰性結果(假陰性)。如我們所知,新型冠狀病毒的主要感染部位位於肺部和下呼吸道,例如肺泡和支氣管。因此,從深咳嗽或支氣管肺泡灌洗液(BALF)中的痰液標本被認為對病毒檢測的敏感性最高。但是,在臨床實踐中,通常使用鼻咽或口咽拭子從上呼吸道收集樣品。收集這些標本不僅對患者感到不舒服,而且需要經過特殊培訓的人員。為了減少侵入性或更容易的採樣,在某些情況下,患者可能會得到口腔拭子,並讓他們從頰粘膜或舌頭擦拭樣品。沒有足夠的病毒RNA,RT-QPCR可以返回假陰性測試結果。在中國湖北省,初始檢測中RT-PCR敏感性僅報告約30%-50%,平均為40%。假陰性的高率很可能是由於採樣不足而引起的。
此外,RT-PCR測試需要訓練有素的人員來執行複雜的RNA提取步驟和PCR擴增程序。它還需要更高水平的生物安全保護,特殊實驗室設施和實時PCR儀器。在中國,需要在BioSafety 2級實驗室(BSL-2)中進行COVID-19檢測的RT-PCR測試,並使用生物安全3級(BSL-3)實踐進行人員保護。根據這些要求,從1月初到2020年2月初,中國武漢CDC實驗室的容量每天只能檢測到幾百例。通常,在測試其他傳染病時,這不是問題。但是,當與2019年COVID等全球大流行打交道時,由於其對特殊實驗室設施或技術設備的要求,RT-PCR可能會被測試數百萬。這些缺點可能會將RT-PCR限制為用作篩查的有效工具,並且也可能導致測試結果報告的延遲。
血清學抗體檢測法
隨著疾病病程的進展,尤其是在中期和晚期,抗體檢測率很高。武漢中央南部醫院的一項研究表明,在19 Covid-19感染的第三週,抗體檢測率可能達到90%以上。同樣,抗體是針對新型冠狀病毒的人類免疫反應的產物。抗體測試比RT-PCR具有多個優點。首先,血清學抗體測試簡單而快速。抗體側流測試可用於護理點,以在15分鐘內提供結果。其次,血清學檢測檢測到的靶標是抗體,該抗體比病毒RNA更穩定。在收集,傳輸,存儲和測試中,抗體測試的樣品通常比RT-PCR的標本更穩定。第三,由於抗體在血液循環中均勻分佈,因此與核酸測試相比,採樣變化較少。抗體測試所需的樣品體積相對較小。例如,10微晶的手指刺血足以在抗體橫向流程測試中使用。
通常,選擇抗體測試作為核酸檢測的補充工具,以提高疾病過程中新型冠狀病毒的檢測率。當抗體測試與核酸測試一起使用時,它可能通過減少潛在的假陽性和假陰性結果來提高診斷CoVID19的測定準確性。當前的操作指南不建議單獨使用兩種類型的測試作為獨立的檢測格式,但應用作合併格式。 [2]
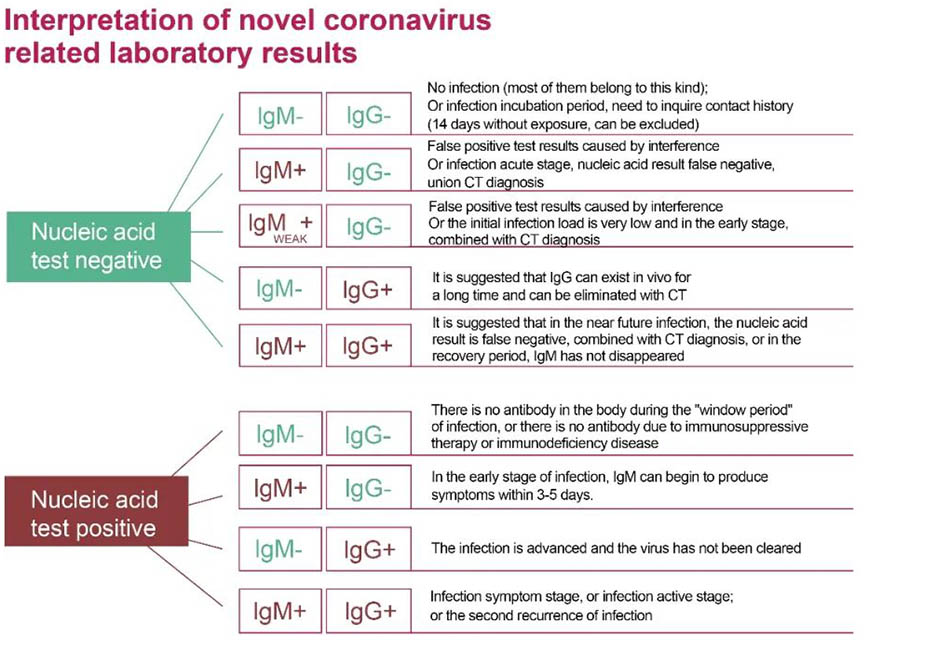
圖2:核酸和抗體測試結果的正確解釋結果用於檢測新型冠狀病毒感染

圖3:Liming Bio-Products Co.,Ltd。 - 新型冠狀病毒IgM/IgG抗體雙重快速測試試劑盒(StrongStep®SARS-COV-2 IgM/IgG抗體快速測試,乳膠免疫色譜學)

圖4:Liming Bio-Products Co.,Ltd。 - Strongstep®新型冠狀病毒(SARS-COV-2)多重實時PCR試劑盒(三個基因檢測,熒光探針方法)。
筆記:這種高度敏感的,即用的PCR試劑盒以凍乾格式(凍乾過程)提供長期存儲。該套件可以在室溫下運輸和儲存,並且穩定一年。每座預用的每個管都包含PCR擴增所需的所有試劑,包括反向轉移酶,TAQ聚合酶,引物,探針和DNTPS底物。用戶可以簡單地通過與模板一起添加PCR級水來簡單地重新構建混合物,然後加載模板,然後再加上模板在PCR儀器上運行放大。
為了應對新的冠狀病毒爆發,Liming Bio-Products Co.,Ltd。迅速努力開發兩個診斷套件,以使臨床和公共衛生實驗室能夠快速診斷Covid-19 Covid-19。這些試劑盒非常適合在新型冠狀病毒爆發迅速擴散的國家和地區進行大規模篩查,並為COVID-19感染提供診斷和確認。這些套件僅在預先宣布的緊急使用授權(PEUA)下使用。測試僅限於根據國家或地方當局法規認證的實驗室。
抗原檢測方法
1。病毒抗原檢測分類為與核酸檢測的直接檢測類別。這些直接檢測方法尋找樣品中病毒病原體的證據,可用於確認診斷。但是,抗原檢測試劑盒的發展需要具有強親和力和高靈敏度的高質量的單克隆抗體,能夠識別和捕獲致病病毒。通常需要超過六個月的時間才能選擇和優化適合用於製備抗原檢測試劑盒的單克隆抗體。
2。目前,直接檢測新型冠狀病毒的試劑仍處於研究和開發階段。因此,尚無抗原檢測試劑盒經過臨床驗證並在市售中可用。儘管以前報導說,深圳的一家診斷公司已經開發了一個抗原檢測試劑盒並在西班牙進行了臨床測試,但由於存在試劑質量問題,因此無法驗證測定的可靠性和準確性。迄今為止,NMPA(前中國FDA)尚未批准任何抗原檢測套件供臨床使用。總之,已經開發了多種檢測方法。每種方法都有其優點和局限性。來自不同方法的結果可用於驗證和補體。
3。產生質量Covid-19測試套件在很大程度上取決於研究和開發過程中的優化。 Liming Bio-Product Co.,Ltd。需要測試套件來滿足嚴格的製造和質量控制標準,以確保它們提供最高水平的性能和一致性。 Liming Bio-Product Co.,Ltd。的科學家在設計,測試和優化體外診斷試劑盒方面具有超過20年的經驗,以確保分析定量的最高效果水平。
在Covid-19的大流行期間,中國政府面臨著國際熱點中對流行病預防材料的巨大需求。 4月5日,在國務院聯合預防和控制機制的新聞發布會上,“加強醫療材料的質量管理並規範市場秩序”,該部對外貿易部的第一級檢查員江恩·範(Jiang Fan)商務說:“接下來,我們將重點放在兩個方面,首先是加快國際社會所需的更多醫療用品的支持,並改善產品的質量控制,監管和管理。我們將為中國對全球流行病的共同做出貢獻,並建立一個為人類提供共同未來的社區。



圖5:Liming Bio-Products Co.,Ltd。的新穎冠狀病毒試劑已獲得EU CE註冊證書
名譽證書


休斯尚
圖6。LimingBio-Products Co.,Ltd.支持Wuhan Vulcan(Houshenshan)Mountain Hospital與COVID-19-19的流行病作鬥爭,並獲得了Wuhan Red Cross的榮譽證書。武漢·瓦肯山醫院(Wuhan Vulcan Mountain Hospital)是中國最著名的醫院,專門治療嚴重的共同治療-19名患者。
隨著小說的冠狀病毒爆發繼續在世界各地傳播,Nanjing Liming Bio-Products Co.,Ltd.正在加緊支持並幫助我們在全球範圍內的創新技術來抗擊這一前所未有的全球威脅。 Covid-19感染的快速測試是應對這一威脅的關鍵部分。我們通過將高質量的診斷平台提供給前線醫療人員的手中,以便人們可以收到所需的關鍵測試結果,從而繼續以重要的方式做出貢獻。 Liming Bio-Products Co.,Ltd。在與Covid-19的大流行戰鬥中所做的努力是為國際社區貢獻我們的技術,經驗和專業知識,以建立一個全球的命運社區。
長按〜掃描並跟隨我們
電子郵件: sales@limingbio.com
網站:https://limingbio.com
發佈時間:5月1日至2020年







