
抽象的
最近,Nanjing Liming Bio-Products Co.,Ltd。(www.limingbio.com)SARS-COV-2 LGM/IgG抗體快速測試套件已獲得巴西國家健康監督局的認證,並獲得了ANVISA認證。同時,SARS-COV-2 RT-PCR和IgM/IgG抗體快速測試試劑盒也列在印度尼西亞的官方推薦採購清單上。同時,Liming Bio strongstep®新加坡健康科學管理局(HSA)批准了新穎的冠狀病毒(SARS-COV-2)多重實時PCR套件,並獲得了HSA證書。

圖片1巴西ANVISA認證
巴西(ANVISA)認證
ANVISA,被稱為Agêncianacional deVigilânciaSanitária,是巴西醫療設備調節器。一家公司有必要在國家健康監督機構安維薩(Anvisa)進行註冊,以便在巴西合法出售醫療設備。要獲得認證,進入巴西的那些醫療設備必須滿足巴西GMP的要求以及巴西當局設定的具體標準。在巴西,根據從低到高的風險水平,IVD醫療設備分為I類,II,III和IV。對於I類和II類產品,採用了卡達斯特羅的方法,而對於III和IV類產品,使用了註冊方法。成功註冊後,ANVISA將發出註冊號,數據將上傳到巴西醫療設備數據庫,此編號及其相應的註冊信息將出現在DOU(Diáriofialialoficial daUnião)上。


圖片2新加坡健康科學管理局(HSA)證書


圖3印度尼西亞的官方推薦採購清單

圖片4 strongstep®SARS-COV-2 IgM/IgG抗體快速測試
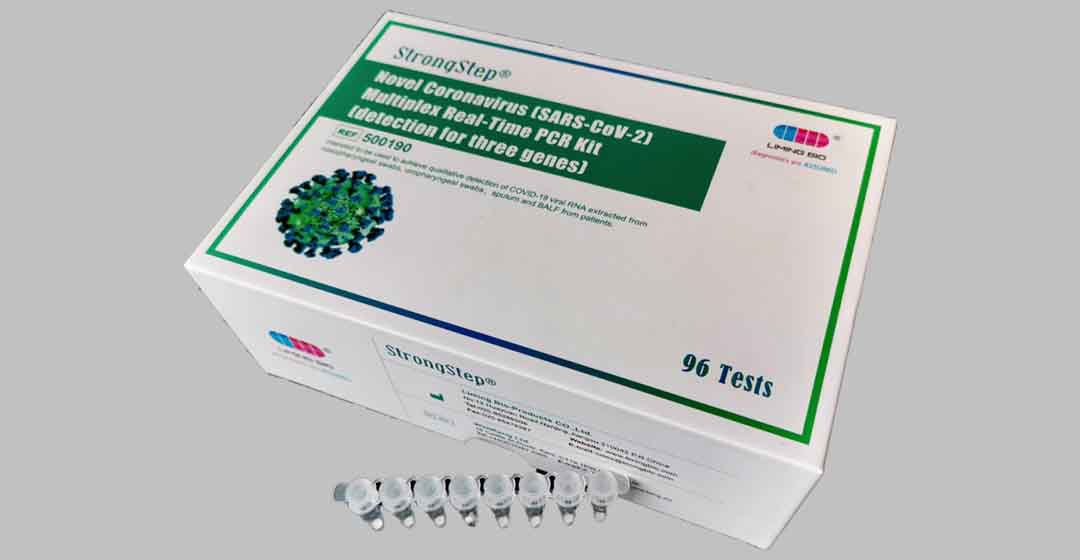
圖片5新穎的冠狀病毒(SARS-COV-2)多重實時PCR套件
筆記:
這種高度敏感的,即用的PCR試劑盒以凍乾格式(凍乾過程)提供長期存儲。該套件可以在室溫下運輸和儲存,並且穩定一年。每個預用的每個管都包含PCR擴增所需的所有試劑,包括反向轉移酶,TAQ聚合酶,引物,探針和DNTPS底物。它只需要添加13ul蒸餾水和5ul提取的RNA模板,然後可以在PCR儀器上運行並放大。
新型冠狀病毒核酸檢測試劑的冷鏈運輸的難度
當常規的核酸檢測試劑以長距離運輸時,需要(-20±5)℃冷鏈存儲和運輸,以確保試劑中的酶的生物活性保持活躍。為了確保溫度達到標準,每盒核酸測試試劑甚至小於50克都需要幾公斤乾冰,但只能持續兩三天。從行業實踐的角度來看,製造商發行的試劑的實際重量小於容器的10%(或遠小於此值)。大部分重量來自乾冰,冰袋和泡沫盒,因此運輸成本非常高。
2020年3月,Covid-19開始在國外大規模爆發,對新型冠狀病毒核酸檢測試劑的需求急劇增加。儘管出口冷鏈中的試劑的成本很高,但由於大量和高利潤,大多數製造商仍然可以接受。
但是,隨著國家針對抗大流行產品的國家出口政策的改善,以及對人類和物流流的國家控制的升級,試劑的運輸時間延長和不確定性,導致了傑出的產品問題通過運輸。延長運輸時間(運輸時間約為半個月非常普遍)會導致產品到達客戶時頻繁的產品故障。這使大多數核酸試劑導出了企業。
PCR試劑的凍乾技術有助於全世界新型冠狀病毒核酸檢測試劑的運輸
凍乾的PCR試劑可以在室溫下運輸和儲存,這不僅可以降低運輸成本,而且還可以避免運輸過程引起的質量問題。因此,凍乾試劑是解決出口運輸問題的最佳方法。
凍乾涉及將溶液冷凍到固態,然後在真空條件下昇華並分離水蒸氣。幹溶質保留在具有相同組成和活性的容器中。與常規液體試劑相比,通過liming生物生產的全成分凍乾的新型冠狀動脈核酸檢測試劑具有以下特徵:
非常強大的熱量穩定性:它可以在56℃時進行60天的支架處理,並且試劑的形態和性能保持不變。
正常的溫度存儲和運輸:無需冷鏈,不需要在低溫之前存儲,在拆開之前,完全釋放冷藏空間。
現成的使用:所有組件的凍乾,不需要係統配置,避免了具有高粘度(例如酶)的組件的損失。
一根管中的多重靶標:檢測靶標涵蓋了新型冠狀病毒ORF1AB基因,n Gene,s基因,以避免病毒Genovariation。為了減少假陰性,人類RNase P基因被用作內部控制,以滿足樣品質量控制的臨床需求。
SARS-COV-2 IgM/IgG抗體快速測試和新型冠狀病毒(SARS-COV-2)多重實時PCR試劑盒(三個基因的檢測)以前在英國標記了CE,現在已被EUA接受和處理美國的FDA。
Nanjing Liming Bio-Products Co.,Ltd.始終將測試套件的質量放在首位,並集中於容量的擴展。該公司將向世界各地的醫療機構提供高質量的Covid-19測試產品和服務,並為全球流行病的預防和控製做出貢獻,以建立一個共同的未來的全球社區。
長按〜掃描並跟隨我們
電子郵件:sales@limingbio.com
網站:https://limingbio.com

發佈時間:7月6日至2020年







